Avastin: storia del farmaco che costava troppo poco
06/03/2014 di Alessandro D'Amato

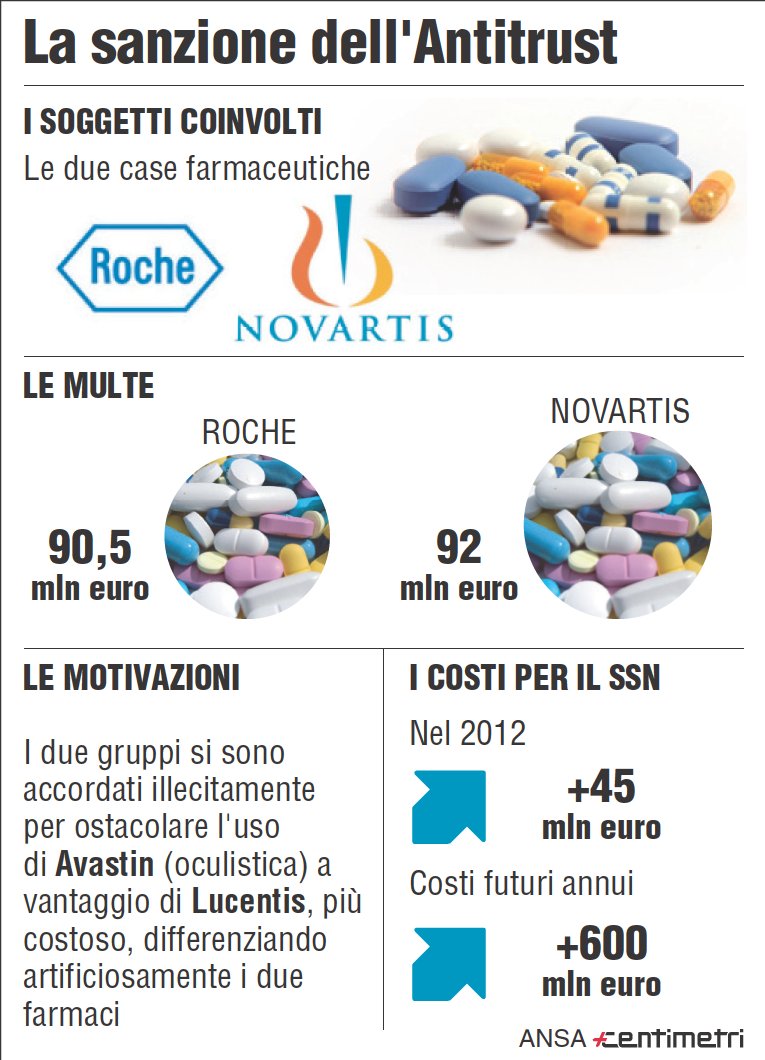
Avastin e Lucentis: attorno a queste due medicine ruota oggi la storia che ha coinvolto Novartis e Roche, multinazionali della farmaceutica multate ieri dall’Antitrust con l’accusa di aver fatto cartello sul prezzo dei due farmaci, cercando di favorire il più costoso. La vicenda Roche-Novartis su Avastin e Lucentis in questa infografica di Centimetri:
ROCHE, NOVARTIS E LA STORIA DELL’AVASTIN – Le due case farmaceutiche dovranno pagare oltre 180 milioni di euro, rispettivamente 90,5 milioni e 92 milioni, per essersi accordate illecitamente sul prezzo, favorendo il farmaco che costava 900 euro rispetto a quello che ne costava 80. Ricorda Repubblica:
L’Antitrust dice che per colpa del cartello il servizio sanitario ha già speso 45 milioni di euro in più, la Società oftalmologica italiana (Soi) stima che circa 100 mila pazienti non possono essere curati perché i costi non sono compatibili con i budget all’osso degli ospedali imposti dalla logica della spending review. E con l’avvocato Riccardo Salomone ha presentato un esposto alla procura di Torino ipotizzando i reati di truffa aggravata e addirittura di corruzione.
Roche e Novartis si difendono:
Sono accuse infondate. I due farmaci sono diversi». Entrambe hanno annunciato che ricorreranno al Tar. Sarà una battaglia. Perché questa è una storia complessa nella quale si intrecciano, come sempre con Big Pharma, la ricerca scientifica e la ricerca dei profitti, la produzione privata e le regole fissate dalle autorità pubbliche competenti, le autorizzazioni e le successive deroghe, la cura delle malattie e la concorrenza tra aziende, gli accordi sottobanco e le strategie di marketing, le lobby. Questa è una storia esemplare.
EH, LO FANNO, LO FANNO! – Sempre su Repubblica Michele Bocci racconta che il metodo che sono accusate di aver utilizzato Novartis e Roche non è affatto una novità:
Non c’è bisogno di arrivare agli estremi del caso Avastin-Lucentis, basta molto meno per aumentare la spesa farmaceutica e quindi i fatturati. E poco male se vecchi medicinali ancora utili escono di produzione o molecole davvero innovative perdono il loro reale valore nel calderone di false o mezze novità. Quel milligrammo ha regalato mesi di nuova giovinezza al Procaptan della Stroder, un farmaco efficace contro l’ipertensione. Quando il brevetto è scaduto e sono entrati sul mercato i generici a base del principio attivo perindopril, il produttore ha avuto un’idea. Ha cambiato i dosaggi da 4 e 8 milligrammi a 5 e 10, di fatto creando un nuovo farmaco. Così quando il medico scrive sulla ricetta Procaptan il paziente non può chiedere al farmacista il generico, come avviene per altri medicinali di marca con il brevetto scaduto, e il sistema sanitario spende 20,69 euro invece di 7,14. Proprio in questo periodo stanno entrando in commercio versioni “low cost” con il nuovo dosaggio del prodotto di marca.
Sulla Stampa invece si riporta la posizione integrale di Roche e Novartis:
«Esistono studi indipendenti eseguiti da organismi internazionali e con dati pubblici che dimostrano un differente profilo di sicurezza dei due farmaci, Lucentis e Avastin – afferma Gaia Panina, direttore medico Novartis -. In nessun modo è possibile costruire in maniera artificiosa delle evidenze. Inoltre sono le autorità regolatorie ad aver deciso in merito. Nel caso dell’Italia è l’Aifa (l’Agenzia italiana del farmaco) a valutare questi studi e decidere se mettere o no in commercio un farmaco. E nel caso specifico, l’unico farmaco che si potrà continuare a prendere è comunque il Lucentis che ha registrato meno eventi avversi». Stessa linea per Roche, l’altra azienda coinvolta: «Siamo obbligati per legge a segnalare appena se ne viene a conoscenza ogni evento avverso si registri a seguito dell’utilizzo di un farmaco in label (indicazioni approvate) o off label (fuori indicazione terapeutica). Sono solo le autorità regolatorie internazionali a decidere dell’opportunità di una modifica del foglietto illustrativo e dell’invio una nota informativa ai medici».
Mentre Luca Pani, direttore dell’Aifa, si difende:
E che dati vi hanno fornito le Regioni?
«Su 44mila pazienti trattati con Lucentis eAvastin sono arrivate informazioni solo su 34. Un quadro desolante della capacità di raccogliere dati sulla sicurezza di queste molecole per uso oftalmico. Ed è chiaro che in un simile quadro di incertezza per la salute dei cittadini e per l’erario Aifa non poteva che agire con la massima cautela».
Altri non ne hanno avuta, accusando Avastin di essere pericoloso per spo- stare le prescrizioni sul farmaco dieci volte più caro…
«Se ci sono intese di cartello che influenzano le informazioni sul piano tecnico e scientifico purtroppo l’Agenzia non ha modo di agire direttamente e sarebbe auspicabile rinforzare la collaborazione con l’Antitrust. Anche perché non è detto che casi del genere non si ripetano in futuro, visto che il mercato globale è cambiato e certi ritorni economici vanno trovati altrove, con il rischio di comportamenti non etici».